炎症性肠病患者罹患结直肠癌的风险显著增加,但结肠炎-癌转化进程中的关键调控分子仍知之甚少。近日,南京大学生命科学学院、医药生物技术全国重点实验室孙洋团队发现组织激肽释放酶1(KLK1)在结肠炎症和癌变过程中逐步下调,其补充能够维护肠黏膜屏障完整性,并抑制结直肠癌发生发展。机制上,KLK1通过调控B1受体介导的成纤维细胞表型转变和细胞外基质重塑发挥保护作用。该研究揭示了结直肠癌新“刹车样分子”—KLK1,为炎症性肠病的防治及结直肠癌的化学预防提供了新靶标。
【研究背景】:
临床挑战:溃疡性结肠炎等炎症性肠病患者长期处于慢性炎症状态,肠屏障持续受损,癌变风险显著增加。
关键问题:结肠炎相关结直肠癌的发生机制复杂,尤其是上皮细胞与成纤维细胞间的相互作用尚未明确。是什么机制推动了“炎症→癌症”的转化?是否存在“刹车样”分子?
研究切入点:组织激肽释放酶(KLK)家族在多种疾病中扮演重要角色,KLK1是激肽-激肽释放酶系统的重要成员,广泛参与炎症调控。KLK1在结肠正常上皮细胞中高表达,但在溃疡性结肠炎和结直肠癌患者中逐渐降低,提示其潜在的“保护因子”样作用。
【主要发现】:
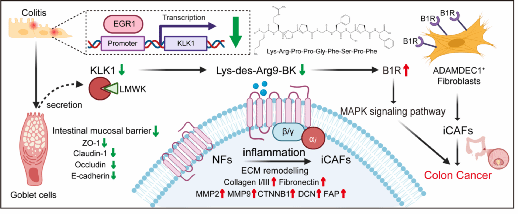
该研究系统揭示了KLK1在炎症性肠病及结直肠癌发生发展中的关键作用。研究发现,随着溃疡性结肠炎、腺瘤到结直肠癌的进展,KLK1在血清和组织中的表达逐渐下降,其缺失会导致肠道屏障受损、炎症加剧,并通过KLK1-[Lys-des-Arg9-BK]-B1R-ECM轴促进成纤维细胞向促癌型表型转化。补充重组KLK1可有效修复黏膜屏障、维持肠道稳态,并显著降低炎症驱动和基因突变驱动的结直肠癌发生风险。
研究意义与展望
首次揭示KLK1是维持肠黏膜屏障和抑制结肠癌变的关键“刹车样分子”。
靶向KLK1-[Lys-des-Arg9-BK]-B1R轴可有效阻止炎症驱动的结肠癌变进程。
临床患者数据提示KLK1水平下降与结肠炎癌进展密切相关。
KLK1有望成为炎症性肠病和结直肠癌防治的重要靶标。
值得一提的是,KLK1(注射用尤瑞克林,国药准字H20052065)具备良好的安全性与应用前景,目前已获批用于卒中的治疗,未来结合类器官、人源化模型及临床队列研究,有望推动KLK1相关治疗在炎症性肠病及炎症相关肿瘤中的个体化应用,为结直肠癌的防治提供新策略。
论文信息
题目:KLK1 as an Epithelial-Specific Brake Inhibits Colorectal Tumorigenesis by Suppressing B1R-Mediated Fibroblast Phenotypic Transition期刊:Advanced Science(2025年8月26日在线发表)原文链接:https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202507063
作者团队
南京大学生命科学学院周莉莎博士生和王美晶博士、刘顺吉硕士生和江苏省中医院顾立梅博士为该论文的共同第一作者,南京大学生命科学学院孙洋教授、上海交通大学附属第六人民医院陈红旗副主任医师、南京中医药大学程海波教授和江苏省中医院凌亭生教授为该论文的共同通讯作者。该研究获得国家重点研发计划、国家自然科学基金、上海市自然科学基金以及江苏省中医院结直肠息肉中西医结合临床医学创新中心基金等资助。
分享到

- 微信

- 朋友圈

- 微博



 1869
1869 电子营业执照
电子营业执照